《饮食中的有机化合物——乙醇》教学设计 山东省济南第十一中学化学组 王芸 【教材分析】 《饮食中的有机化合物》是新课标高中化学必修2模块中的有机化学部分,本节在整个第三章中的地位非常突出,是从生活中的营养物质切入具体的有机物,按“结构-性质-重要作用-回归人体中的作用”这样的模式来学习。通过本节的学习,不仅可使学生认识一些重要的烃的衍生物的典型代表物,而且可以丰富他们的生活常识,提高自身的科学素养。并且让学生在初中有机物常识的基础上,能进一步从结构的角度,加深对有机物和有机化学的整体认识。本节是整个第3节的第一课时,本节课设计成功,可以极大的激发学生的学习兴趣,为以后的学习铺平道路。 【教学目标】 1、知识与技能 通过科学探究,学生掌握乙醇的组成和主要性质。学会从官能团出发,分析有机物的化学性质。 2、过程与方法 通过创设生活情景,引导学生结合生活常识来学习,并帮助学生建立“结构——性质——用途”的有机物学习模式。 3、情感态度与价值观 通过学生的实验探究,体验从未知到已知的乐趣,激发学生学习化学的热情。并且通过模型的拼凑,提高学生的动手能力,培养实践的意识。另外,提高安全意识,不喝酒,不酒后驾驶。 【学情分析】 乙醇是日常生活中常见的有机物,在初中化学中学生已经接触过乙醇,对乙醇的分子式、存在和应用有了一定的了解,而且高一学生正处在求知欲强、好胜心强、兴趣广泛,他们学习思维的广阔性、深刻性、逻辑性和创造性明显增加,学习动机比较稳定,具有一定的分析问题、解决问题的能力。但是在自主学习方面,虽然经过了高一一学期的训练,仍然显得能力不足,需要在教学中注重这方面培养。 【教学重难点】 重点:1、探究乙醇的组成和结构, 2、了解有机物结构决定性质, 3、掌握乙醇与金属钠的反应和氧化反应。 难点:探究乙醇取代反应和氧化反应的反应机理。 【教学策略】 实验探究、模型认知、多媒体辅助教学 【课时安排】 1课时 【教学过程设计】 环节内容 | 教师活动 | 学生活动 | 设计意图 | 创设情境 | 【导入新课】 通过播放各式各样酒图片和对酒文化的讲解,引出生活中的有机化合物-乙醇 | 思考、回答: 乙醇在日常生活中的应用 | 激发学生兴趣,引入新课—乙醇 | 引导 | 乙醇的用途这么广泛,与生活联系密切,那我们当然要对乙醇有更多的了解。 | 乙醇的物理性质 | 【实验感知】指导学生进行实物感知,利用乙醇除去涂在手上的记号笔墨水,分析桌面上的乙醇试剂瓶,小组之间通过观察和翻阅资料从色味态等方面,相互讨论学习,总结出乙醇的物理性质。 | 小组汇报结果: 乙醇是无色、有特殊香味的液体。乙醇易挥发,沸点为78.5℃,密度比水小,能够溶解多种有机物和无机物,能与水以任意比互溶。 | 培养从生活中获取化学知识,相互学习,取长补短的良好学习习惯 | 设疑 | 乙醇既然作为一种有机物,要学习乙醇,必须要知道乙醇的结构。 | 思考: 乙醇的分子式,结构式,结构简式是怎么样的呢? | 引入新问题 | 科学探究乙醇的结构 | 【提出假设】 教师给出乙醇的分子式为C2H6O,学生利用桌面上的彩色橡胶分子结构模型,以小组为单位,尝试拼出C2H6O可能的结构。教师巡视,给予学生必要的指导。 | 积极思考,动手操作,实践出真知: 学生利用桌面上的材料,根据已有的对有机物成键结构的认识,积极拼出C2H6O可能的结构 | 培养学生的动手能力和实践出真知的探索精神 | 【模型分析】CH3CH2OH结构中有与H2O相似的结构,乙醇是否和水有相似的性质呢 | 引导学生思考水与钠的反应 | 培养学生运用类比分析的能力。 | 【科学验证】学生做乙醇与金属钠反应的创新实验。取一定量的乙醇试液,加入一块用滤纸吸干煤油,并且切成小块的金属钠,把金属钠放入乙醇中。把产生的气体通过爆鸣实验验证。引导学生自己总结实验现象,并分析乙醇的结构式。 | 思考、集体回答: 1、 观察到的实验现象:金属钠在乙醇的底部,有气泡产生,有爆鸣声。 2、 乙醇的结构与水、煤油中的烃结构的的异同。 | 培养学生的观察能力和总结分析能力 | 【得出结论】 从实验验证中,可以得到乙醇的结构。教师给出乙醇的分子式,结构式,结构简式、球棍模型和比例模型。 | 分析归纳,填写学案: 学生自己总结出乙醇的结构,得到成功的快感。再把知识点进行归纳记录。 | 培养学生记录学到的知识的良好学习习惯 | 总结乙醇的结构式提出官能团的概念 | 提出重要的概念:官能团。同时开始强调分析有机物的性质必须从官能团出发,提出结构决定性质,官能团决定性质的理论。 | 学生在学案上记录知识点: 官能团:决定有机化合物的化学特性的原子或原子团。 | 引导学生从有机物的结构和官能团入手来分析一个有机物的性质 | 过渡 | 正是因为乙醇含有羟基这个官能团才使得它跟烷烃在化学性质上有很大的差异,那么羟基究竟给乙醇带来什么独特的性质呢?下面就要来学习 | 倾听,思考: 乙醇有那些化学性质 | 引导学生思考羟基引起的乙醇哪些独特的性质 | 乙醇与金属钠的反应 | 通过PPT动画演示乙醇与钠反应的过程。引导学生利用乙醇的模型模拟反应的发生。引导学生认识反应的机理,断键的位置。 | 思考,实践: 学生动手模拟反应的发生,知道从官能团——羟基,分析反应断键的位置和反应的机理。 | 通过直观的动画和模型,让学生从宏观上理解微观的有机反应的机理 | 乙醇的氧化反应 | 引导学生回忆乙醇的燃烧反应,指导学生书写乙醇和氧气反应的方程式,总结反应的实验现象 | 书写乙醇和氧气的反应方程式 | 提高学生综合利用知识的能力 | 能力提升 | 乙醇燃料在生活中的应用,讲述酒精火锅和酒精燃料飞机、乙醇汽油 | 思考关注乙醇的能源价值 | 提高学生关注能源、关注化学与生活联系的意识和能力 | 乙醇的催化氧化反应 | 以小组为单位,小组同学完成乙醇催化氧化成乙醛的实验。 [实验步骤](1)点燃酒精灯,拿一根洁净的铜丝在酒精灯外焰灼烧(2)把灼热的铜丝放入盛有乙醇的试管中(量为1/4试管)(3)观察铜丝颜色,闻液体的气味 引导学生观察实验现象和记录实验现象。 | 动手完成实验、观察和记录实验现象、小组汇报实验现象: 1、 铜丝颜色的变化,从红到黑到红。 2、 红到黑发生了铜氧化成氧化铜的反应 3、 黑到红的过程伴随着刺激性气味的产生 | 锻炼学生的动手能力和总结归纳实验现象的能力 | 探究乙醇的催化氧化反应的机理 | 教师给出乙醇被氧化成乙醛的反应方程式,小组同学利用桌面上乙醇的模型,比较乙醇和乙醛组成上的异同,探索乙醇催化氧化反应的机理。 | 思考、分析、动手操作、汇报结果: 1、 小组同学动手完成模型的拼凑。 2、 让一位学生当小老师,上黑板给其他同学说明反应的机理是:断开羟基上的氧氢键和与羟基相连的碳上的碳氢键。 | 培养学生的动手能力和语言表达能力。引导学生进一步理解官能团决定性质 | 知识归纳 | 理解铜丝在反应中的作用是催化剂,通过方程式的相加,写出总反应方程式。 | 倾听、观看ppt、在学案上记录 | 培养学生知识的归纳能力 | 知识迁移,能力提升 乙醇与强氧化剂的反应 | 乙醇与重铬酸钾溶液的反应:观看ppt上的图片,是交警检测司机是否酒驾的图片,图片上用的仪器是传统的检测仪,里面装的是重铬酸钾溶液,当司机呼出的空气包含乙醇,乙醇与重铬酸钾溶液接触,溶液就从橙色变成绿色,乙醇被直接氧化成乙酸,从而达到检测的效果。除了重铬酸钾以外,乙醇跟高锰酸钾等强氧化剂也能直接生成乙酸。引导学生思考为什么不能饮酒过量,对人体产生什么影响 | 思考、讨论 | 联系生活,让学生懂得化学的价值。从真实情境中教育学生不能有酒驾的违法行为培养分析、归纳、知识迁移、发散思维的能力 | 课堂 小结 | 1、知识总结 2、方法总结 | 1、知识总结: (1)乙醇的结构 (2)乙醇与金属钠反应 (3)乙醇的氧化反应 2、方法总结:有机物的官能团决定性质,分析性质与机理时必须从官能团入手。 | 知识升华 培养归纳能力 | 能力提升 | 掌握了一定知识后,通过一定量的练习进行巩固和提升。 | 思考,回答 | 巩固知识,培养共同学生的学风 | 课后作业 | 1、查阅资料,用糯米发酵,自酿米酒。 2、根据收集的有关酒的资料,结合本节课学习的知识,选择研究小课题进行探究。(酒的发展史、酒的酿造、酒的结构与性质、酒文化和酒的用途等) | 认真完成 | 巩固知识 |
【板书设计】 饮食中的有机化合物——乙醇 一、 物理性质 二、 分子结构 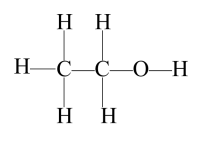 三、 化学性质  1、2CH3CH2OH+2Na 2CH3CH2ONa +H2 1、2CH3CH2OH+2Na 2CH3CH2ONa +H2
 2、CH3CH2OH+3O2 2 CO2+3H2O 2、CH3CH2OH+3O2 2 CO2+3H2O
 2CH3CH2OH+O2 2CH3CHO+ 2H2O 2CH3CH2OH+O2 2CH3CHO+ 2H2O
【教学反思】 本节课的教学设计为通过“小组合作”的学习模式贯穿整个教学过程。笔者在课堂上设置了5次的小组活动,5个小组合作学习活动下来占用了整个课堂的1/3~1/2的时间。 这本是一个以学生的“学”为主体,让整个课堂气氛活跃,热闹非凡的教学设计,但是细听下来,有些小组中,某些同学只听不说,某些同学只说不听。有些小组则天南地北,东拉西扯。本来“小组合作学习”在发挥学生的主体性地位、彰显学生的个性和发展学生的能力等方面起着重要作用。但如果任其讨论,不加引导,可能会取得反效果。 因此,在教学过程中,教师必须首先提出需要解决的主要问题,然后引导学生主动讨论,在讨论中加深对所学知识的理解,理解后学会用科学严谨的语言表达自己的想法,这个过程下来学生会对所学所论的知识留下非常深刻的印象。特别是在有机化学的教学中,有机物的组成,反应的机理是有机化学的核心内容。另外,通过小组之间对分子式的讨论,对分子结构的摸索和拼凑,对反应机理的解读,可以让学生快速的识记碳链的链接方式和反应的机理。而且在学生讨论的过程中,教师应该对所涉及的问题多加解释,多加引导避免学生天马行空。
|